Zuletzt aktualisiert am 10. März 2021 um 22:36
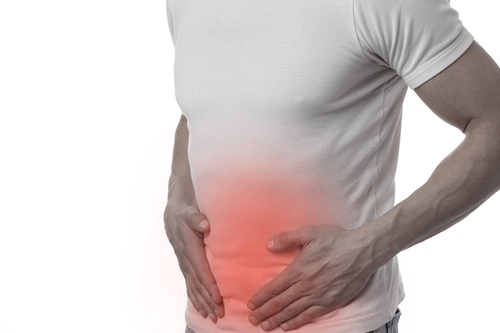
Colitis ulcerosa ist eine chronisch-entzündliche Darmerkrankung, bei der der Dickdarm betroffen ist. Sie zählt zu den Autoimmunerkrankungen. Die Dickdarmschleimhaut entzündet sich, es bilden sich Geschwüre (Ulcera). Blutiger Durchfall und Bauchkrämpfe sind die Folge.
Colitis ulcerosa – eine Zusammenfassung
- Colitis ulcerosa ist eine Autoimmunerkrankung des Dickdarms. Dabei kommt es aus verschiedenen Gründen zu einer Autoimmunreaktion und einer chronischen Entzündung der oberen Dickdarmschleimhaut.
- Zu den Colitis ulcerosa Symptomen zählt hauptsächlich häufiger, blutiger Durchfall mit Schleim und Eiter, darüber hinaus auch Bauchkrämpfe und Müdigkeit.
- Deutschlandweit sind etwa 200.000 Menschen von der Krankheit betroffen. Zusammen mit Morbus Crohn ist es die häufigste chronisch-entzündliche Darmerkrankung (CED).
- Je nach Schweregrad (Lokus) und aktuellem Schub setzt sich die Therapie aus Entzündungshemmung, Schmerztherapie und Immunsuppressiva zusammen. Eine Heilung sieht die schulmedizinische Therapie nicht vor.
- Mittels gesunder Ernährung, Nahrungsergänzungen, Kräutern und gesunder Lebensführung ist es möglich die Anzahl und Dauer von Colitis ulcerosa Schüben zu verringern und Remission zu erreichen. Auch kann die Remission dadurch jahrelang erhalten bleiben. Hierbei bietet sich eine Kombination aus Schulmedizin und Naturheilkunde an.
Was ist Colitis ulcerosa?
Wörtlich übersetzt bedeutet Colitis ulcerosa „Dickdarmentzündung mit Geschwürbildung“. Es ist eine Autoimmunerkrankung des Darms und wird ausschließlich im Dickdarm lokalisiert. Colitis ist neben Morbus Crohn die häufigste chronisch-entzündliche Darmkrankheit (CED). Bei Autoimmunerkrankungen kommt es zur Fehlleitung des Immunsystems. Als Folge werden körpereigene Zellen als Feind erkannt und massiv bekämpft.
Bei Colitis ulcerosa kommt es zu einer Autoimmunreaktion sowohl gegen die obere Darmschleimhaut als auch gegen die Darmbakterien, die sich darin eingenistet haben. Früher ging die Wissenschaft davon aus, dass es sich um eine chronische Entzündung handelt, bei der es zur Infektion der oberen Darmschleimhaut durch Bakterien kommt und gegen die die Immunzellen vorgehen 2-3.
Mittlerweile weiß man jedoch, dass es sich um eine Autoimmunerkrankung handelt. Dafür sprechen: das Auftreten von Autoantikörpern gegen die obere Darmschleimhaut, der chronische und schubweise Verlauf der Erkrankung und die allgemeinen Symptome wie Fieber und Gelenkschmerzen.
Colitis ulcerosa beginnt im Mastdarm, breitet sich von dort auf den gesamten Dickdarm aus und kommt am Übergang zum Dünndarm zum Stehen. In 10 % der Fälle entwickelt sich daraus die Autoimmunerkrankung Morbus Crohn, die den gesamten Magen-Darm-Trakt betrifft.
In Deutschland sind etwa 200.000 Menschen von Colitis ulcerosa betroffen, so viele wie von Morbus Crohn. Es gibt genauso viele männliche wie weibliche Betroffene.
Durch die chronische Entzündung der Dickdarmschleimhaut und die Immunreaktion bilden sich Geschwüre (Ulzerationen), die im gesamten Dickdarm zu finden sind.

Colitis ulcerosa tritt je nach Ausbreitung und Lokus in verschiedenen Formen auf. Zunächst veranschaulicht das Bild den Aufbau des Dickdarms.
Colitis ulcerosa Formen
Proktitis:
Bei dieser Form ist nur der Mastdarm betroffen.
Pankolitis:
Diese Form tritt bei 20 % aller Betroffenen auf. Der gesamte Dickdarm ist betroffen.
Proktosigmoidis ulcerosa:
Hier reicht die Krankheit bis in die Sigma-Schleife.
Linksseitige Colitis:
Die Entzündung reicht bis zur letzten Krümmung (linke Flexur), diese Form tritt bei 30 – 40 % aller Erkrankten auf.
Fulminante Colitis ulcerosa:
Es kommt zu einem toxischen Megakolon, Darmbruch und schweren Darmblutungen. Bei dieser Form muss sofort ein Krankenhaus aufgesucht werden.
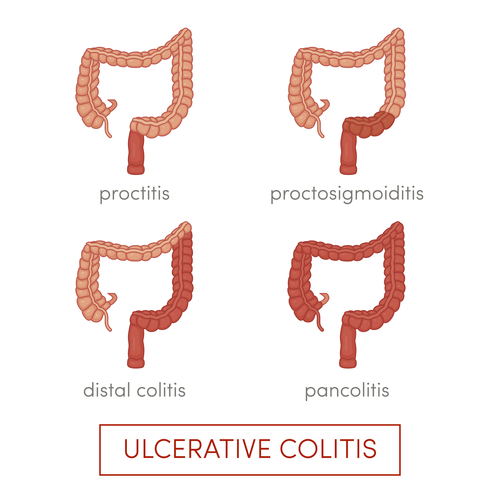
Bei jedem zweiten Betroffenen verläuft die Krankheit leicht bis mäßig schwer. Nur einzelne Teile des Dickdarms sind dann betroffen.
Doch wie unterscheiden sich Colitis ulcerosa und Morbus Crohn?
Unterscheidung zwischen Colitis ulcerosa und Morbus Crohn – ein Überblick
Beide Autoimmunerkrankungen sind die wichtigsten chronisch-entzündlichen Darmerkrankungen (CED). Beide betreffen in Deutschland etwa 200.000 Menschen. Die Erkrankungen unterscheiden sich aber deutlich, wie die Tabelle aufzeigt:
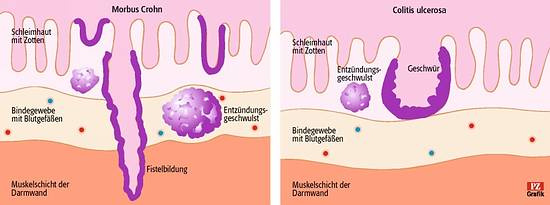
Tabelle: Die Unterschiede zwischen Morbus Crohn und Colitis ulcerosa
| Morbus Crohn | Colitis ulcerosa |
| Kein zentraler Entzündungsherd, der gesamte Magen-Darm-Trakt ist betroffen. | Wenige, intensive Entzündungsherde. |
| Ausbreitung erfolgt im gesamten Magen-Darm-Trakt. | Ausbreitung erfolgt ausschließlich im Dickdarm. |
| Alle Schichten der Darmwand sind betroffen. | Nur die obere Schicht der Darmschleimhaut ist betroffen. |
| Wenig Blut und Schleim im Stuhl. | Bluter und schleimiger Durchfall. |
| Fistel-Bildung. | Keine Fistelbildung, aber Geschwüre (siehe nachfolgendes Bild) und Pseudopolypen. |
| Geringeres Darmkrebsrisiko als bei Colitis ulcerosa. | Deutlich gesteigertes Dickdarmkrebsrisiko im Vergleich zur nicht betroffenen Bevölkerung. |
In den nachfolgenden Abbildungen werden die Unterschiede abgebildet:

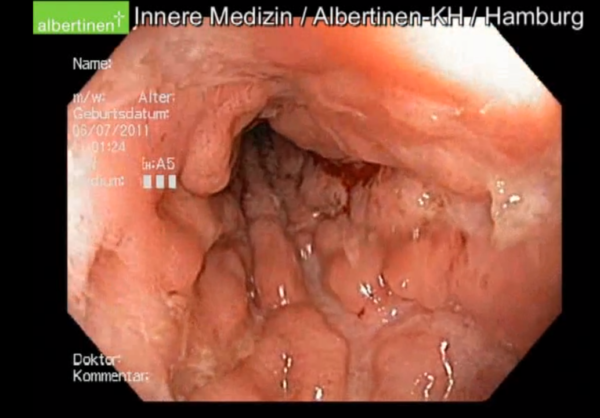
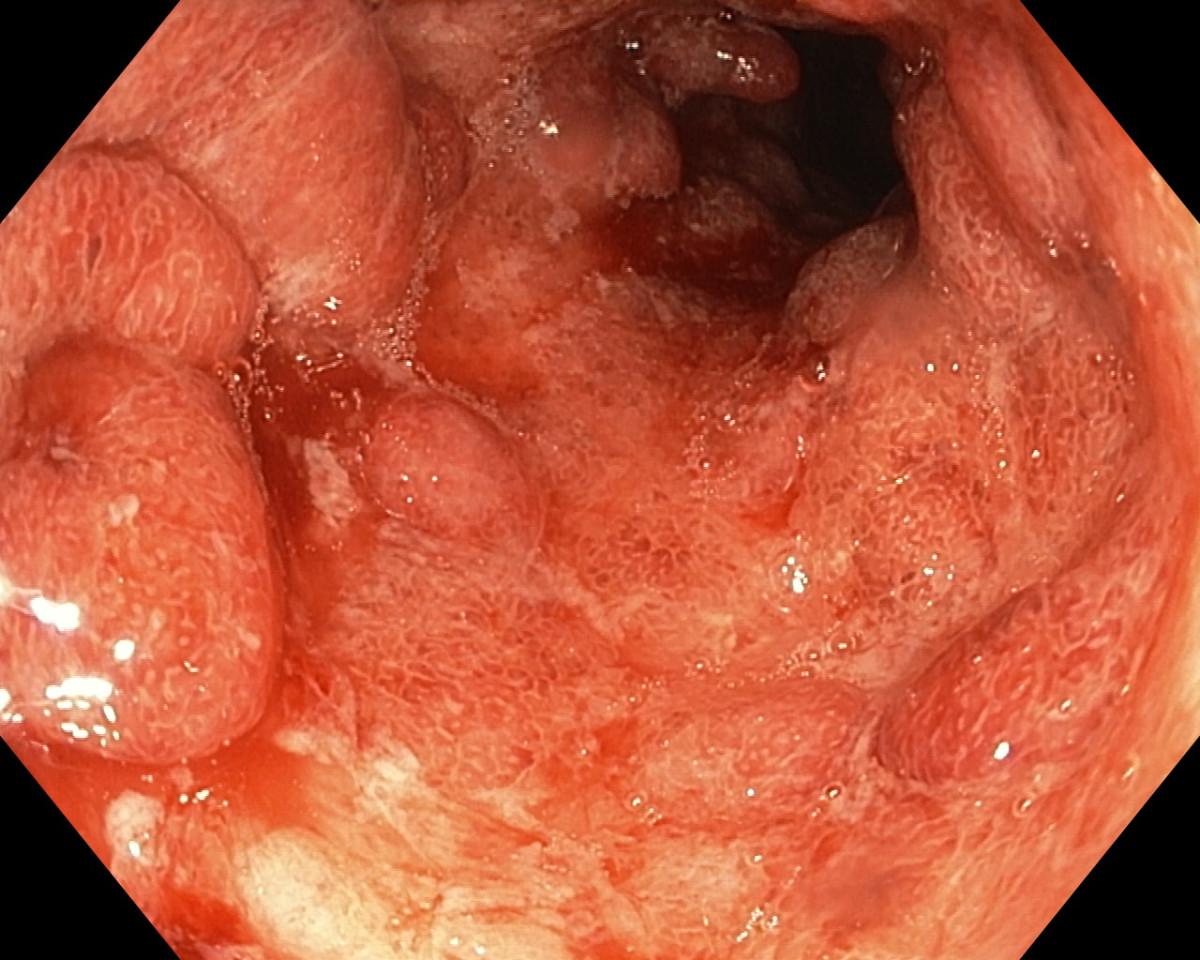
Colitis ulcerosa – Symptome und Beschwerden
Wie äußert sich Colitis ulcerosa?
Bei der chronisch-entzündlichen Darmerkrankung zeigen sich entsprechende Symptome:
- Blutiger Durchfall mit Schleim und Eiter (Leitsymptom für die Diagnose).
- Chronische Müdigkeit, besonders während eines Schubs.
- Unerklärbarer Gewichtsverlust.
- Auftreten der Krankheitssymptome in Schüben.
- Bauchschmerzen, besonders nach Mahlzeiten.
- Bauchkrämpfe am linken Unterbauch.
- Häufiger Stuhlgang (bis 20x täglich während eines akuten Schubs).
- Das Gefühl, ständig auf die Toilette zu müssen.
- Das Gefühl, nie entleert zu sein.
Die genannten Symptome und Beschwerden sind besonders in der Bauchregion spürbar, genauer im Dickdarm. Es treten zudem Symptome außerhalb des Magen-Darm-Traktes auf.
Extraintestinale Manifestierungen:
- Gelenkschmerzen.
- Entzündung am Auge (Uveitis).
- Hautveränderung und Hautentzündungen.
- Wachstumsstörungen bei Kindern.
- Während eines akuten Schubs: Fieber, Herzrasen, Schwäche, Blutarmut.
Wichtige Komorbiditäten bei Colitis ulcerosa
- PSC (Primär sklerosierende Cholangitis): kleine Gallengänge in der Leber entzünden sich, verengen und vernarben. Eine Hepatitis (Leberentzündung) kann die Folge sein. Betroffene haben ein um 500 % erhöhtes Risiko für Dickdarmkrebs.
- Multiple Sklerose.
- Morbus Bechterew.
- Entzündungen am Auge.
- Osteoporose.
- Morbus Crohn.
Die benannten Symptome im Dickdarm und außerhalb des Darms sprechen für Colitis ulcerosa. Die Beschwerden müssen nicht gemeinsam auftreten und können einen unterschiedlichen Schweregrad aufweisen. Häufiger Stuhlgang und blutiger und schleimiger Durchfall als Leitsymptom sind entsprechende Symptome. Treten diese schubweise und längerfristig auf, empfiehlt sich ein Arztbesuch, um eine mögliche Colitis ulcerosa Diagnose zu stellen.
Diagnose von Colitis ulcerosa
Wer diagnostiziert Colitis ulcerosa?
Der erste Ansprechpartner kann ein Hausarzt, Heilpraktiker oder funktioneller Mediziner sein. Häufen sich die Verdachtsmomente für Colitis ulcerosa, werden Sie an einen Gastroenterologen überwiesen. Gastroenterologen verfügen (neben funktionellen Medizinern) über die nötigen Kenntnisse und Methodik, eine Colitis ulcerosa Diagnose festzustellen. Diese wird nach den Kriterien und Leitlinien des DCCV1 und DGVS durchgeführt.

Körperliche Untersuchung
- Abtasten des gesamten Unterbauches: Wichtige Symptome sind hier Druckschmerz und Schmerz am linken Unterbauch.
- After-Inspektion: Wichtige Symptome sind eine Rötung sowie Entzündung des Enddarms.
Blutentnahme
Die folgenden Blutwerte sind nicht zwangsläufig erhöht, erleichtern aber im Falle einer Auffälligkeit die Diagnose:
- CRP: Universeller Entzündungsmarker im Körper. Bei Autoimmunerkrankungen, chronischen Infektionen und Entzündungen dauerhaft erhöht.
- Blutsenkungsgeschwindigkeit (BSG): Bei Colitis ulcerosa ist diese erhöht.
- GGT (Gamma-Glutamyl-Transferase): Bei einer Schädigung der Leber erhöht.
- Alkalische Phosphatase (AP): Bei chronischer Entzündung sowie metabolischer Azidose (Übersäuerung) erhöht.
- Eisen und Ferritin: Besonders während eines aktiven Schubs stark erniedrigt.
- Hämoglobin: Während eines aktiven Schubs erniedrigt (Anämie).
- Transaminase: Bei Leberschäden infolge der Krankheit erhöht.
- Nieren Gesundheit: GFR (Leistung der Niere) erniedrigt.
- Cholestase bzw. Gelbsucht eventuell nachweisbar (erhöhtes Bilirubin).
Stuhlprobe
Diese Methode ist unschön. Für den Arzt ist sie aber wichtig, um eine mögliche Diagnose abzuklären. Zudem werden durch die Stuhlprobe andere Ursachen für die Symptome ausgeschlossen, wie eine infektiöse Colitis. Im Stuhl sind einige Marker nachweisbar:
- Laktoferrin: Protein, das nur in Immunzellen vorkommt. Ist es im Stuhl nachweisbar, liegt höchstwahrscheinlich eine chronische Darmerkrankung vor (auch bei Zöliakie, Leaky Gut Syndrom, Morbus Crohn nachweisbar).
- Calprotectin 65: Ähnlich Laktoferrin in Immunzellen, spricht für eine Immunreaktion und Schäden im Darm.
- Blut im Stuhl und Eiter nachweisbar.
- Neopterin im Stuhl nachweisbar.
Darmspiegelung (Koloskopie) und Ultraschall
Koloskopie und Ultraschall sind die wichtigsten Methoden, um eine Diagnose zu stellen. Ultraschall wird nur von erfahrenen Ärzten angewandt, um das Ausmaß der Entzündung im Darm einschätzen zu können. Bei der Darmspiegelung (Koloskopie) wird mittels Abführmittel der Darm komplett entleert und anschließend eine Sonde mit einer Kamera rektal eingeführt.
Mit der Kamera kann der Arzt Struktur, Aufbau und Entzündung des Dickdarms überprüfen sowie Gewebeproben entnehmen. Durch die Gewebeproben ist eine Unterscheidung zu Morbus Crohn leichter durchführbar.
Ab acht Jahren nach der Diagnose totaler Colitis (Pankolitis) und ab 15 Jahren nach der Diagnose linksseitiger Colitis empfiehlt es sich eine jährliche Koloskopie machen zu lassen. Colitis ulcerosa Patienten haben nämlich ein erhöhtes Dickdarmkrebs-Risiko.
Mittels der genannten Methoden ist mit hoher Wahrscheinlichkeit eine Colitis ulcerosa Diagnose feststellbar. Nach der Diagnose endet für die Betroffenen häufig eine lange Odyssee zu verschiedene Ärzten, um die Ursache für Symptome und Beschwerden zu finden. Mit Colitis ulcerosa liegt eine Autoimmunerkrankung des Darms vor. Durch moderne Wissenschaft, Medikamente und weitere Erkenntnisse ist die Lebensqualität der Betroffenen nur bedingt eingeschränkt. Durch kombinierte Therapien gelangen immer mehr Patienten in dauerhafte Remission.
Ist Colitis ulcerosa heilbar?
Nach der Diagnose wird von Ärzten mitgeteilt, dass Colitis ulcerosa eine Autoimmunerkrankung ist, ein Leben lang bleibe und somit unheilbar sei. Doch ist die Erkrankung wirklich unheilbar?
Heilung ist ein schwieriger Begriff in der Medizin, insbesondere im Bezug auf Autoimmunerkrankungen. Denn Heilung impliziert nicht nur eine völlige Symptomfreiheit (Remission), sondern eine Regeneration des Körpers bis zur Wiederherstellung des Ausgangszustands.
Bei Autoimmunerkrankungen ist das betroffene Gewebe durch die jahrelange Autoimmunreaktion teilweise so stark beschädigt, dass eine komplette Regeneration nicht möglich ist. Insofern ist es bei Autoimmunerkrankungen im Vergleich zu beispielsweise Virusinfekten schwer, von Heilung zu sprechen. Ziel einer guten Therapie, auch bei Colitis ulcerosa, sollte Remission, also völlige Symptomfreiheit, sein.
Um die Lebensqualität zu steigern, die Symptome zu unterdrücken und die Langzeitschäden zu minimieren, ist es empfehlenswert, direkt nach der Diagnose mit einer geeigneten Colitis ulcerosa Therapie fortzufahren.
Therapie und Medikamente bei Colitis ulcerosa
Die schulmedizinische Therapie bei Colitis ulcerosa ist abhängig vom Schweregrad und vom Lokus der Erkrankung. Zur Schulmedizin sei im Allgemeinen gesagt, dass sie nicht auf eine Remission oder auf Heilung abzielt. Stattdessen soll den Betroffenen durch Symptomunterdrückung, Zeit und Lebensqualität gewährt werden.
Die Ursachen der Erkrankung, die bis heute nicht gänzlich bekannt sind und über die nur spekuliert werden kann, sind mit Schulmedizin nicht ausreichend beachtet. Umso wichtiger wird die Kombination aus Schulmedizin und Naturheilkunde, um eine bestmögliche und integrative Behandlung zu bieten. Wissenschaftliche Studien bestätigen diesen kombinierten Ansatz.
Um den Betroffenen Zeit zu gewähren, die Symptome zu unterdrücken und die Lebensqualität zu steigern, ist der Einsatz der schulmedizinischen Therapie ratsam. Besonders während eines akuten Schubs.

Akuter Schub
Hier werden Entzündungshemmer wie zum Beispiel Kortison verabreicht. Bei einer Intoleranz gegenüber Kortison wird auf Immunsuppressiva wie 6-Mercatorpurin, Azathioprin, Cyclosporin und selten auf Tacrolimus gewechselt. Auch auf Biologika wie Infliximab, Adalimumab und Golimumab wird ausgewichen.
Proktitis
Wenn lediglich der letzte Abschnitt des Dickdarms betroffen ist, führen Betroffene über Zäpfchen oder Einläufe den Wirkstoff 5-Aminosalicylsäure (5-ASA) rektal ein. Dieser Stoff ist eng mit ASS (Acetylsalicylsäure, Aspirin) verwandt 12. Reicht der Wirkstoff nicht aus, wird zusätzlich Kortison zur Unterdrückung der Immunantwort eingesetzt.
Linksseitige Colitis
Ist die Colitis weiter ausgebreitet, verschreibt der Arzt orales 5-ASA. Es wird als Granulat oder Tablette mit einem Trägermaterial eingenommen und erst im Dickdarm freigesetzt. Die Präparate sind unter den Namen Sulfasalazin und Mesalazin bekannt 20-22. Die längerfristige Anwendung dieser Wirkstoffe birgt ein erhöhtes Risiko für Schäden an den Nieren sowie an Pankreatitis zu erkranken.
Fulminanter Schub
Da dieser Zustand lebensbedrohlich ist, muss der Patient umgehend in einem Krankenhaus behandelt werden. Es wird eine Kortisoninfusion gelegt und Immunsuppressiva eingenommen.
Erhaltungstherapie (Remissionstherapie)
Die Remissionstherapie kommt in den Phasen zwischen Schüben zum Einsatz. Da Kortison längerfristig zahlreiche Nebenwirkungen auf den Organismus entfaltet, wird hier auf den Einsatz von Kortison verzichtet. Stattdessen wird niedrig dosiertes 5-ASA als Mesalazin eingenommen. Bei einer Mesalazin-Intoleranz kann die Krankenkasse zusätzlich Probiotika verschreiben lassen.
Weitere Ansätze
- In allen Krankheitsphasen reduzieren Flohsamen die Intensität und Häufigkeit der Durchfälle. Sie sollten jedoch nur eingesetzt werden, wenn sich im Darm keine Stenosen (verengte Blutgefäße) gebildet haben.
- Bei leichter bis mittlerer Colitis ist in den letzten Jahren Rosiglitazon immer mehr zum Einsatz gekommen 23-24. Hierbei handelt es sich um einen PPAR-γ -Agonisten, der die Kommunikation zwischen Immunsystem und Darmflora verbessert und so zu einer starken Entzündungslinderung beiträgt.
Nebenwirkungen von Medikamenten
Entzündungshemmer, Biologika und Immunsuppressiva sind effizient bei der Symptomunterdrückung und können in einzelnen Fällen zu Remission (Mesalazin) führen. Jedoch sind diese Medikamente immer mit Nebenwirkungen verbunden. Niedrige Dosierungen bei dauerhafter Medikamenteneinnahme und ein bedachter Einsatz senken das Risiko für Langzeitschäden oder Komplikationen wie Nierenschäden, Hepatitis oder Pankreatitis.
Eine dauerhafte Immununterdrückung hat eine Erhöhung des Krebsrisikos im gesamten Körper zur Folge (Bekämpfung von Tumorzellen ist eine wichtige Aufgabe des Immunsystems). Zudem steigt das Risiko für chronische Infektionen. Es ist empfehlenswert, sich immer über die Nebenwirkungen der verschriebenen Medikamente aufklären zu lassen. Falls Sie mit einem Präparat nicht zufrieden sind, lasen sie sich Alternativen erklären.
Besonders die im Zusammenhang mit Colitis ulcerosa am häufigsten verschriebenen Medikamente Mesalazin (Nierenschäden, Pankreatitis) und Azathioprin (Schwindel, Übelkeit, Kopfschmerzen, Nierenschäden) sind mit verschiedenen Nebenwirkungen verknüpft. Dies gilt auch für andere Immunsuppressiva wie Cyclosporin 25 und Biologika.
Operation bei Colitis ulcerosa
Bei jahrelanger Verschlimmerung der Krankheit, bei schweren Komplikationen, schweren Blutungen oder Dickdarmkrebs kann eine Operation nötig werden. Dabei werden zur Entfernung von Entzündungsherden Teile des Dickdarms und im schlimmsten Fall der komplette Dickdarm entfernt.
Wenn der Dickdarm ganz entfernt wird, wird ein Pouch (Verbindung zwischen Dünndarm und After) oder ein Stoma (künstlicher Dickdarmausgang) gelegt. Bitte beachten Sie, dass diese Operation nur durchgeführt werden sollte, wenn keine andere Möglichkeit besteht. Denn durch die Entfernung entfallen die vielseitigen und wichtigen Einflüssen der Darmflora auf die menschliche Gesundheit.
Andererseits bleiben Auslöser für die Autoimmunerkrankung bestehen und das Immunsystem bleibt chronisch aktiv und entzündet. Es kann dann passieren, dass sich die Autoimmunerkrankung auf ein anderes Gewebe (zum Beispiel den Dünndarm, siehe Morbus Crohn) oder den Pouch ausweitet (Pouchitis)62. Daher sollte die komplette Entfernung des Dickdarms nur angewandt werden, wenn keine andere Möglichkeit besteht.
Impfungen bei Colitis ulcerosa?
Da Patienten zumeist längerfristig Immunsuppressiva einnehmen und die Wahrscheinlichkeit für Infektionserkrankungen erhöht ist, empfehlen sich Impfungen gegen die saisonale Grippe, Pneumokokken und Hepatitis B.
Kinder und Colitis ulcerosa
Auch Kinder können von der Erkrankung betroffen sein. Auf die Gabe von Kortison bei Kinder ist zu verzichten. Es kann sonst zu Wachstumsstörungen kommen.
Welche Schmerzmittel bei Colitis ulcerosa?
Die meisten rezeptfreien Schmerzmittel behindern aufgrund einer starken entzündungslindernden Wirkung im Darm mögliche Reparaturmechanismen und es kommt in vielen Fällen zu einer Verschlimmerung der Symptome. Lediglich Aspirin stellt laut einer Studie eine Option dar 29. Jedoch hat auch Aspirin den entscheidenden Nachteil, aufgrund seiner blutverdünnenden und anti-inflammatorischen Wirkung mögliche Darmblutungen zu verstärken, und damit Reparaturmechanismen zu verhindern. Außerdem weisen alle Schmerzmittel Nebenwirkungen auf, was eine längerfristige Einnahme problematisch macht.
Die Frage nach den richtigen Schmerzmitteln kann daher nicht beantwortet werden und bleibt eine Frage, die nur der jeweils behandelnde Arzt beantworten kann. Eine Entzündungshemmung über andere Medikamente wie Mesalazin oder Biologika und besonders über Anpassungen in der Lebensführung erscheint als die sinnvollere Herangehensweise.
Die Colitis ulcerosa Ursachen und was in der Dickdarmschleimhaut bei Colitis ulcerosa passiert, wird nachstehend erläutert.
Colitis ulcerosa Ursachen
Was passiert bei Colitis ulcerosa?
Wie es zur Krankheit Colitis ulcerosa kommt und was in der Dickdarmschleimhaut passiert:
Veränderte Darmschleimhaut
Die obere Schicht des Dickdarms ist zu dünn. Studien zufolge ist diese Schicht bei Betroffenen der Colitis ulcerosa bis zu 70 % dünner als bei Nicht-Betroffenen 1. Die Darmwand ist daher anfälliger für Entzündungen und die Einwanderung von bakteriellen Erregern wird begünstigt. Dies wird außerdem durch die verringerte Bildung antibakterieller Stoffe der dünnen Darmschleimhaut erleichtert.
Mitochondriale Dysfunktion
Die Kraftwerke in den Zellen der Darmschicht (Mitochondrien) weisen häufig Schäden auf. Dieser Prozess geht mit einer chronischen Entzündung einher und verschlimmert die Gesamtsituation weiter. Es ist nicht bekannt, welches Ereignis zuerst auftritt: die Entzündung, die Infektion oder die mitochondriale Dysfunktion. Als gesichert gilt, dass alle drei Faktoren bei Colitis ulcerosa vorliegen.
Kommunikation zwischen Immunsystem und Darmflora geht verloren
Durch genetische Prädisposition, Entzündungen und weitere genannte Ursachen kommt es zu einer geringeren Ausschüttung von Vitamin D, PPAR-γ und IL-10. Diese drei sind wichtige Signalstoffe für die Kommunikation zwischen Darmflora und Immunsystem. Geht diese Kommunikation verloren, wandern vermehrt Bakterien in die Schleimhaut ein 7. Immunzellen starten schneller eine Entzündungsreaktion und es kommt zu einer Autoimmunreaktion gegen die Dickdarm-Schleimhaut.
Autoimmunreaktion gegen Dickdarm-Schleimhaut
Mittlerweile gilt es als erwiesen, dass Colitis ulcerosa eine Autoimmunerkrankung ist. Bei 70 % der Betroffenen sind Autoantikörper gegen Typ VII-Kollagen, ein charakteristisches Kollagen in der oberen Darm-Schleimhaut, nachweisbar 18. Zudem kommt es zu einer erhöhten Bildung des Enzyms MMP9 (Matrix-Metalloprotease-9), um die Schleimhaut aktiv abzubauen. Die Autoimmunreaktion geht folglich mit einer zu dünnen Schleimhaut einher. Jedoch ist nicht bekannt, was zuerst auftritt: die zu dünne Schleimhaut oder die Autoimmunreaktion.
Zu wenig antimikrobielle Stoffe
Durch genannte Faktoren kommt es zu einer verringerten Bildung von antimikrobiellen Peptiden, Antikörpern (IgA)9 und Mukus (Schleim). Dies erleichtert die Einwanderung von Bakterien in die Schleimhaut.
Dysbalance der Darmflora
Bei Betroffenen der Colitis ulcerosa liegt ein starkes Ungleichgewicht in der Darmflora vor.
Ungleichgewicht der Immunzellen
Bei der Autoimmunerkrankung liegen vermehrt entzündungsfördernde Immunzellen (TH1, TH17)5 und zu wenige entzündungslindernde Immunzellen (regulatorische T-Zellen) vor.
Zusammengefasst heißt das, dass die Dickdarmschleimhaut zu dünn ist, entzündet, infiziert. Sie wird von Immunzellen angegriffen und hat zu wenige Antioxidantien. Es kommt zu einer schwachen Kommunikation zwischen Immunsystem und Darmflora. Man könnte meinen, Colitis ulcerosa ist eine Autoimmunreaktion gegen die Dickdarm-Schleimhaut als auch gegen die eigene Darmflora, die sich in dieser Schleimhaut eingenistet hat.
Kommentar: Bei näherer Betrachtung fallen zudem Ähnlichkeiten mit Neurodermitis auf – nur, dass es sich hier um den Dickdarm, nicht um die Haut handelt.
Diese Zusammenhänge wurden erst in den letzten 10 Jahren bestätigt. Vorher wurde Colitis ulcerosa nicht als Autoimmunerkrankung, sondern als chronisch-entzündliche Darmerkrankung (ohne Autoimmunreaktion) eingestuft.
Ursachen für die Erkrankung
Ursachenforschung ist bei Colitis ulcerosa ein wichtiger Faktor und soll nachstehend ausführlich erläutert werden. Sie erklärt, warum die Erkrankungszahlen immer mehr zunehmen83-84.
Genetik
Genetische Veranlagungen spielen eine wichtige Rolle bei der Entstehung der Krankheit. Jedoch weniger als oftmals behauptet.
Der genetische Faktor wird mit etwa 20 % auf die Entstehung der Krankheit beziffert 80. Es wurden bereits über 140 genetische Polymorphismen festgestellt, die mit einem erhöhten Auftreten der Erkrankung in Verbindung stehen. Die meisten dieser Mutationen und genetischen Veränderungen laufen auf einen veränderten Vitamin D-Stoffwechsel und eine schlechtere Immun-Darmflora-Kommunikation durch die stark reduzierte Bildung von PPAR-γ und IL-10 hinaus.
Hygiene
Ende der Fünfzigerjahre war Colitis ulcerosa noch nicht bekannt, heute betrifft die Krankheit bereits etwa 200.000 Menschen in Deutschland. Europaweit sind es circa drei Millionen. Die steigende Hygienisierung der westlichen Gesellschaft wird als ein Auslöser benannt.
Die Hygienehypothese 79 sagt aus, dass Kinder während ihrer Entwicklung mit Mikroorganismen aus der Umwelt in Kontakt kommen sollten. Das Immunsystem ist bei diesen Kindern noch nicht ganz ausgereift. Daher ist der Kontakt mit Mikroorganismen wichtig, um ein gesundes Immunsystem, eine gesunde Darmflora und auch eine gute Kommunikation zwischen beiden aufzubauen 35.
Wachsen Kinder in einer zunehmend sterilen Umgebung auf, bewegen sich wenig in der Natur und werden nicht gestillt (wichtige Quelle für Präbiotika), kann sich das Immunsystem nicht vollständig ausbilden und reifen. So kommt es im frühen Erwachsenenalter (nach dem Auswachsen) immer verstärkter zu Autoimmunerkrankungen. Ein erster Lösungsansatz ist Kinder wieder mehr zum Spielen in die Natur zu schicken.
[su_spoiler title=“Stillen und Colitis ulcerosa“]
In Ergänzung zur Hygienehypothese konnte gezeigt werden, dass Kinder und Babys, die lange gestillt wurden, ein deutlich geringeres Risiko aufweisen, an Colitis ulcerosa zu erkranken. Stillen ist wichtig, damit Stoffwechsel und Immunsystem des Babys gut ausreifen können und sich eine gesunde Darmflora bildet. Zudem wird über die Muttermilch Nährstoffmängeln vorgebeugt.
[/su_spoiler]
Umweltgifte
Eine weitere Erklärung für den Zuwachs an Colitis-Betroffenen ist die Zunahme von Belastungen des menschlichen Körpers durch Umweltgifte. Diese Umweltgifte lagern sich im Körper ab. Der Darm ist einer der ersten Interaktionspunkte.
Ungesunde Ernährung
In den letzten 60 Jahren wurde die Ernährung in der westlichen Gesellschaft zunehmend industrialisiert. Der Verzehr von Trans-Fettsäuren, tierischen Produkten aus Massentierhaltung und chemischen Zusatzstoffen im Allgemeinen hat stark zugenommen.
Leaky Gut Syndrom
Das Leaky Gut Syndrom, also ein undichter und löchriger Darm, scheint zur Krankheit beizutragen. Es kommt zu mikroskopisch kleinen Löchern im Darm (vor allem im Dünndarm), durch die Toxine und Krankheitserreger in den Stoffwechsel und in den Blutkreislauf gelangen können. Allergien, chronische Entzündungen und Autoimmunerkrankungen werden hierdurch begünstigt. Colitis ulcerosa könnte eine direkte Folge davon sein.
Nährstoffmangel
Nährstoffmängel scheinen ebenfalls zur Entstehung der Krankheit beizutragen 60. Zwar sind Nährstoffmängel auch eine direkte Folge der Erkrankung, weil die Aufnahme derselben beeinträchtigt ist, aber einige Nährstoffmängel scheinen die Krankheit zu begünstigen. Die fettlöslichen Vitamine A, D, E sowie ein Mangel an Antioxidantien scheint eine wichtige Rolle zu spielen 67-70.
Ungleichgewicht in der Darmflora
Ein Ungleichgewicht in der Darmflora scheint die Krankheit ebenfalls stark zu begünstigen. Dies kann durch eine ungesunde Ernährung, zu wenige Präbiotika und zu wenige Probiotika (lebensfähige Mikroorganismen in Nahrungsmitteln) ausgelöst werden.
Risikofaktoren für Colitis ulcerosa
Übergewicht: Übergewicht begünstigt eine chronische Entzündung des Körpers, was mit dem Aufkommen verschiedener Autoimmunerkrankungen in Verbindung gebracht wird.
Stress: Stress steht mit fast jeder Autoimmunerkrankung in Verbindung. Der Einfluss bei Colitis ulcerosa ist als schwächer einzustufen wie beispielsweise bei Hashimoto Thyreoiditis. Dennoch ist er auch bei der Darmerkrankung prägnant 26. Betroffene scheinen besonders häufig unter Trennungsängsten zu leiden.
Zusammengefasst lässt sich über die Ursachen und Risikofaktoren für Colitis ulcerosa folgendes festhalten:
Genetik + Umwelt + Darmflora = Colitis ulcerosa
Mit praktischen Hinweise für den Alltag, Ratschlägen zur Ernährung, Nährstofftherapie und Naturheilkunde kann sich die Krankheit stark verbessern (wissenschaftlich bewiesen) und in Remission übergehen.
Ernährung bei Colitis ulcerosa
Das Ziel einer gesunden Colitis ulcerosa Ernährung ist, die Entzündungen im Darm und Immunsystem zu lindern und eine ausgewogene Darmflora wiederherzustellen. Außerdem soll die Kommunikation im Darm über Aktivierung von PPAR-γ und Interleukin 10 (IL-10) wiederhergestellt werden.
In den Massenmedien sowie in offiziellen ärztlichen Leitlinien wird immer wieder betont, dass kein erwiesener Zusammenhang zwischen einzelnen Ernährungsformen und der Entstehung von Colitis ulcerosa besteht. Das ist richtig.
Es wird jedoch verschwiegen, dass bestimmte Nahrungsmittel, Nährstoffe und bestimmte Ernährungsformen zu einer starken Verbesserung der Colitis und zu einer Remission führen können 17,30-31. Wissenschaftlichen Studien dazu existieren, haben aber noch nicht ihren Weg in die Ärzteschaft und Öffentlichkeit gefunden.
Während eines akuten Schubs verzehren viele Betroffene erfahrungsgemäß weniger Kaffee und scharfe Gewürze. Als Faustregel zur Colitis ulcerosa Ernährung gilt: je gesünder die Ernährung gestaltet wird, desto schneller sind Betroffene von akuten Schüben befreit und desto kürzer sind die Schübe an sich.
In jedem Fall empfiehlt es sich, ein Ernährungstagebuch zu führen. So können Sie die Entwicklung der Krankheit über die Zeit und in Abhängigkeit von bestimmten Ernährungsformen, Nährstoffen und Nahrungsmitteln dokumentieren.
Wissenschaftliche Studien beweisen wieder und wieder, dass die Ernährung bei Colitis ulcerosa einen wichtigen Einfluss auf die Gesundheit, das Immunsystem und die Symptomatik hat. Eine Remission in vielen Fällen möglich ist 17,30-31.
Empfohlene Ernährungsform bei Colitis ulcerosa
2016 wurde eine kleine klinische Studie durchgeführt, in der eine spezielle Ernährungsform an Patienten mit Colitis beziehungsweise Morbus Crohn getestet wurde. Diese Ernährungsform wurde mit einer Nährstofftherapie ergänzt und für elf Wochen aufrechterhalten. Elf Wochen später waren 70 % der Betroffenen in Remission 19.
Wie ist das möglich? Welche Ernährungsform war das, die so effizient zu einer langanhaltenden und schnellen Remission bei Betroffenen führte?
Bei dieser Ernährungsform handelt es sich um das Paleo-Autoimmunprotokoll. Das Paleo-Autoimmunprotokoll ist eine Ernährungsform, die speziell für Autoimmunerkrankte entwickelt wurde. Sie zielt auf die maximale Aufnahme von Nährstoffen, eine maximale Entzündungslinderung und die konsequente Vermeidung von Allergenen sowie Reizstoffen ab. Die Ernährungsform ist eine Weiterentwicklung der Paleo-Ernährung (Steinzeiternährung), die sich am Ernährungsplan unserer Vorfahren aus der Steinzeit orientiert. Paleo-Ernährung gilt als eine der nährstoffreichsten und gesündesten Ernährungsformen.
Das Paleo-Autoimmunprotokoll hat sich bei vielen Autoimmunerkrankungen, besonders bei Colitis ulcerosa als sehr wirkungsvoll herausgestellt. Zudem finden Sie hier eine Lebensmittelliste zum Herunterladen und Ausdrucken. Das Paleo-Autoimmunprotokoll ist die empfehlenswerte Ernährungsweise bei Colitis ulcerosa.
In weiteren Studien wurde erfasst, welche Nahrungsmittel mit einer Verbesserung oder einer Verschlimmerung der Krankheit in Verbindung gebracht werden können. Die folgenden Nahrungsmittel können unabhängig vom Paleo-Autoimmunprotokoll oder als Teil der neuen Ernährungsform in Ihren Ernährungsalltag eingebaut werden. Halten Sie Veränderungen im Ernährungstagebuch fest.

Empfehlenswerte Nahrungsmittel bei Colitis ulcerosa
- Fisch 50-55 (aus Wildfang): kein Thunfisch, Schwertfisch oder Königsmakrele aufgrund der Schwermetallbelastung.
- Bio-Fleisch und Bio-Eier: reich an CLA, ein Stoff, der mit einer Verbesserung der Colitis in Verbindung gebracht wird 52-53.
- Fermentierte Nahrungsmittel wie Sauerkraut, Kimchi, Joghurt, Kombucha, Apfelessig.
- Probiotika 38-43: gut untersucht wurde das Präparat VSL#3 39).
- Knochenbrühe34: reich an Kollagen und entzündungslindernden Glukosaminoglykanen.
- Grünes Gemüse: besonders Blattgemüse wie Spinat, Feldsalat, Löwenzahn und Wildkräuter 49.
- Beeren: besonders Blaubeeren 33 und Aroniabeeren 55.
- Pilze, besonders Shiitake, Austernpilz, Reishi und Löwenmähne
- Fernöstlichen Gewürze: wie beispielsweise Ingwer 48, Kardamom, Fenchelsamen und Kurkuma.
- Cranberries 61.
- Granatäpfel 36-37: auch als Granatapfelextrakt möglich).
Zusatz: Low-Carb oder High-Carb bei Colitis?
Die Tendenz in wissenschaftlichen Studien geht dahin, dass weder eine kohlenhydratreiche noch eine sehr fettreiche Ernährung bei Colitis ulcerosa wichtig ist. Ein ausgewogenes Verhältnis der Makronährstoffe scheint zielführend zu sein.
Nicht zu empfehlende Nahrungsmittel bei Colitis Ulcerosa, die mit einer Verschlechterung der Symptomatik in Verbindung stehen
- Glutenhaltiges Getreide (besser eine glutenfreie Ernährung) 10.
- Zucker 32.
- Fruchtsäfte.
- Fast Food.82
- Industrielle Speiseöle wie Sonnenblumenöl, Rapsöl, Sojaöl.
- Salz und salzreiches Essen (auch Wurst und manche Käsesorten)<sup81.
- Hülsenfrüchte.
- Alkohol.
- Milchprodukte.
- Honig.
- Zitrusfrüchte und Steinobst (austesten, ob es vertragen wird).
- Zwiebelgewächse und Kohl (austesten, ob es vertragen wird).
Zusammen mit dem Paleo-Autoimmunprotokoll haben sich in wissenschaftlichen Studien und in der Praxis die genannten Nahrungsmittel bewährt.
SCD – Specific Carbohydrate Diet
Zudem hat sich die Vermeidung bestimmter Nahrungsmittel bewährt, zu denen neben Zucker und Honig auch blähende Obst- und Gemüsesorten zählen. In klein angelegten Studien sogar mit starker Auswirkung 13-16.
Diese Methode ist als SCD bekannt und obige Ratschläge zu Lebensmittelverwendungen und -vermeidungen enthalten dies bereits. Bei Obst, besonders Steinobst und Südfrüchte, sollten Sie beobachten, was Sie vertragen und was weniger. Hier macht ein Austesten Sinn, da die Verträglichkeiten individuell sind.
Ein Ernährungstagebuch zu führen, hilft die Auswirkung bestimmter Nahrungsmittel auf die Symptomatik zu untersuchen und festzuhalten.
Die Colitis ulcerosa Ernährung wird durch weitere Methoden aus der Naturheilkunde ergänzt, die sich in der Praxis und in wissenschaftlichen Studien bewährt haben.
Naturheilkunde bei Colitis ulcerosa
Ähnlich wie bei der Ernährung ist hier das zelluläre Ziel, die Entzündungen im gesamten Körper und im Immunsystem zu lindern. Zudem ist die Wiederherstellung der Kommunikation zwischen Darmflora und Immunsystem über die Stimulierung von PPAR-γ und IL-10 wichtig.

Kräutertherapie bei Colitis ulcerosa
In den folglich zitierten Studien wurde mit ätherischen Ölen gearbeitet. Der orale Konsum von ätherischen Ölen bei Colitis ist nicht ratsam, da es zu einer Reizung kommen kann. Die ätherischen Öle sind sehr hoch konzentriert. Der Konsum dieser Kräuter als Tee, Kräuterextrakt oder beim Kochen empfiehlt sich jedoch und ist mit weniger Nebenwirkungen verbunden.
Potenziell hilfreiche Kräuter bei Colitis ulcerosa:
- Basilikum75.
- Patchouli77.
- Rosmarin74.
- Schafgarbe.
- Große Käsepappel (Wilde Malve).
- Ringelblume.
- Fenchel.
- Oregano73.
Nahrungsergänzungsmittel bei Colitis ulcerosa
Wie bereits beschrieben, hängt Colitis ulcerosa in der Entstehung mit bestimmten Nährstoffmängeln zusammen. Durch die chronische Darmentzündung kommt es zum erneuten Auftreten einiger Nährstoffmängel, da die Aufnahme von Nährstoffen in den Körper behindert wird. Werden diese Nährstoffmängel behoben, ist mit einer Besserung der Symptomatik zu rechnen. Bitte reden Sie mit Ihrem behandelnden Arzt oder Therapeuten, in welcher Form Nährstoffe am besten zugeführt werden können. Falls die orale Gabe keine ausreichende Effektivität bietet, kann besonders bei der Gabe von fettlöslichen Vitaminen, B-Vitaminen, Eisen und Selen über eine intravenöse Gabe (Spritze) nachgedacht werden.
Folgende Nahrungsergänzungsmittel und Nährstoffe stehen mit einer Besserung der Symptomatik bei Colitis ulcerosa in Verbindung und sind häufige Mangelnährstoffe.
Fettlösliche Vitamine + Calcium67-70
Vitamin A, Vitamin D, Vitamin E und Vitamin K2, zusammen mit einer Kalziumgabe (250-500 mg) verbessert den Knochenstoffwechsel und beugt Osteoporose vor. Außerdem werden dadurch viele Aspekte des Immunsystems und der Darmschleimhaut beeinflusst. 25 % aller Colitis-Patienten leiden an der Osteopathie, der Vorstufe von Osteoporose 66.
Tagesbedarf fettlöslicher Vitamine:
- Vitamin A (10.000 I.U.).
- Vitamin D (ca. 5.000 I.U., mehr Informationen hier: Vitamin D).
- Vitamin E (20 mg, 400-1000 I.U.).
- Vitamin K2 (200 µg).
Die Wichtigkeit von Vitamin D
Vitamin D wurde im Zusammenhang mit Colitis ulcerosa bereits ausführlich erforscht. Es konnte wiederholt gezeigt werden, dass die Schwere der Symptome und die Häufigkeit und Dauer der Schübe mit dem Vitamin D-Spiegel im Blut zusammenhängt 71-72. Daher sollte Vitamin D eine besondere Beachtung finden. Studien zeigen, dass Colitis-Patienten meist einen starken Vitamin D-Mangel aufweisen und es bei einem Blutspiegel von 50-70 ng/ml zu einer starken Verbesserung kommt.
Vitalpilz Extrakte
Heilpilze unterstützen die Verdauung, regenerieren die Darmwand und regulieren die Darmflora. Besonders bewährt haben sich Reishi Extrakt und Löwenmähne Extrakt. Diese können auch im Schub eingenommen werden.
Eisen
Bei einem Eisenmangel und Colitis wird in offiziellen Ratgebern 1 von einer anfänglichen Gabe von 100 mg Eisen pro Tag berichtet. Der Eisenwert wird dabei streng überwacht, bis ein gesunder Blutspiegel erreicht wird. Der sonst übliche Tagesbedarf von Eisen liegt bei 20-30 mg.
Vitamin B12
Auch hier kann es zu Mängeln kommen, falls die orale Gabe nicht anschlägt, wird eine intravenöse Gabe von 1000 µg wöchentlich empfohlen. Weiterhin empfehlen viele offizielle Leitstellen bei Vitamin B-Mangel beziehungsweise einer Prophylaxe die Gabe eines hoch dosierten Vitamin B-Komplexes.
Selen
100-200 µg Selen täglich haben sich in Studien als hilfreiche Unterstützung bei Colitis erwiesen 46-47,28.
N-Acetyl-Cystein
In einer Studie an Schweinen konnte N-Acetyl-Cystein zu einer starken Linderung der Symptome und zu einer verbesserten Darmgesundheit beitragen 57-58. Dies würde einer Dosis von 2-3 g täglich bei Menschen entsprechen und ist bei chronisch-entzündlichen Erkrankungen empfehlenswert.
Curcumin
Curcumin ist einer der effizientesten Wirkstoffe in der Nährstofftherapie bei Colitis ulcerosa. Die Therapie mit Mesalazin wird in vielen Studien unterstützend mit Curcumin durchgeführt und verbessert die Remissionsraten sehr stark 22. 1 g Curcumin, aufgeteilt auf 2 Dosen täglich, ist auch ohne Begleitstoff effektiv.
Weihrauchharz
Neben Curcumin ist Weihrauchharz eines der stärksten pflanzlichen Extrakte bei Colitis ulcerosa. Eine Studie fand heraus, dass 3x täglich 300 mg Extrakt aus Weihrauchharz bei Colitis-Patienten eine Remissionsrate von 70 % bewirkte 59. Durch eine Kombination mit Curcumin könnte diese Wirkung zusätzlich verstärkt werden.
EGCG (Grüntee-Extrakt)
Dieser Extrakt aus grünem Tee ist ähnlich effektiv wie Curcumin und stellt die Darmgesundheit zu einem bestimmten Teil wieder her. Die Kombination von Curcumin/Weihrauchharz und Selen ist in einer Studie als wertvolles Präparat beschrieben worden 27-28.
Melatonin
1-2 mg Melatonin abends könnte die innere Uhr von Patienten wiederherstellen, Entzündungen lindern und zu einer Symptomverbesserung führen.
Ginsengpulver
Ein Teelöffel Ginsengpulver wurde in Studien ebenfalls als potenziell hilfreich bewertet 64. Eine Ergänzung könnte zudem wirkungsvoll Stress abbauen und die Nebenniere stabilisieren.
Resveratrol
1 g Resveratrol (Polyphenol aus roten Weintrauben) täglich hat ähnliche Wirkungen wie EGCG und Curcumin und könnte Betroffenen stark helfen.
Lecithin
Die stark geschädigte Dickdarmschleimhaut weist bei Colitis-Patienten einen zu niedrigen Gehalt an Lecithin (Phosphatidylcholin) auf. In einer Studie konnte die Gabe von 3 g Lecithin täglich zu einer starken Verbesserung der Darmgesundheit und der Symptomatik führen und ist allgemein empfehlenswert 21. Der Wirkstoff wird erst im Dickdarm freigesetzt.
Kombinierte Gabe aus Omega-3-Fettsäuren50-55 und Gamma-Linolensäure (Nachtkerzenöl/Borretschöl)
Beide Stoffe führen zu einer starken Entzündungslinderung und einer besseren Kommunikation der Immunzellen mit der Darmflora. Die Kombination aus beidem erwies sich in Studien wirkungsvoller als die alleinige Gabe 52-53.
Welche Intervention ist die beste? Viele Studien haben sich mit der Verbesserung der Colitis Ulcerosa Symptome durch bestimmte Nahrungsmittel oder Nahrungsergänzungsmittel/Nährstoffe beschäftigt und diese als wirkungsvoll eingestuft.
Das verwirrt auf den ersten Blick. Wichtig ist, zunächst einen Überblick über die aktuelle Ernährung zu erlangen und mit einer gesünderen und an Colitis angepassten Ernährung, idealerweise mit dem Paleo-Autoimmunprotokoll, eine erste Verbesserung der Krankheit zu erreichen. Die Naturheilkunde mit Kräuter- und Nährstofftherapie ist anschließend eine gute Ergänzung.
Welche Nahrungsergänzung bei Ihnen nun am besten wirkt, ist nicht vorhersehbar und bedarf der individuellen Austestung. Studien weisen darauf hin, dass es mehrere Wege mit Nahrungsergänzungsmitteln gibt:
- Die Beseitigung der Nährstoffmängel über fettlösliche Vitamine, Eisen, Selen, B-Vitaminen und N-Acetyl-Cystein ist eine gute Grundlage mit der Nährstofftherapie zu starten. Dies ist bei Nährstoffmängeln grundsätzlich empfehlenswert.
- Ein nächster Schritt könnte dann die Austestung von antientzündlich wirkenden Extrakten wie Curcumin, EGCG, Lecithin und Weihrauchharz sein, unterstützt durch eine Kombinationsgabe von Omega-3-Fettsäuren und Gamma-Linolensäure (Nachtkerzenöl).
Reden Sie mit Ihrem Arzt oder Therapeuten über diese Nährstoffe und zeigen Sie ihm die im Quellenverzeichnis verlinkten Studien. Überzeugen Sie Ihren Arzt oder Therapeuten von der Wirksamkeit einiger Präparate. Heilpraktiker, Naturheilkundler und funktionelle Mediziner wissen meist besser über diese Nährstoffpräparate Bescheid und können Ihnen gute Beratung bieten.
Eine gesunde Lebensführung bei Colitis ulcerosa ist wichtig. Alltag und Lebensweise beeinflussen und verbessern die Krankheitssymptomatik.
Gesunde Lebensführung bei Colitis ulcerosa
Einige Maßnahmen im alltäglichen Leben können zu einer Verbesserung der Gesundheit beitragen. Sie sind Teil der gesunden Lebensführung und bieten sich an, um abseits von Ernährung, schulmedizinischer Therapie und Naturheilkunde für eine Verbesserung der Krankheit zu sorgen.

Innere Uhr
Bei Autoimmunerkrankungen kommt es in vielen Fällen zu einer Schädigung der inneren Uhr, auch bekannt als Chronobiologie. Die innere Uhr hat bedeutende Auswirkungen auf das Immunsystem.
Stressreduktion
Stress ist eine zentrale Ursache für viele Autoimmunerkrankungen und wurde auch bei Colitis ulcerosa mit einer Verschlechterung der Krankheit in Verbindung gebracht. Stressbewältigung und Stress abbauen sind wichtige Bausteine, um im Alltag der Krankheit entgegenzuwirken 11. In den hinterlegten Beiträgen erfahren Sie weitere Informationen zum Thema Stressreduktion.
Schlaf
Gesunder Schlaf ist wichtig, damit sich Darm und Immunsystem nachts regenerieren können. Auch zur Entzündungslinderung ist es wichtig. Betroffene berichten sehr häufig von schlechtem und unzureichendem Schlaf.
Yoga
Ein Zusammenhang zwischen einer Verbesserung der Symptomatik und Yoga konnte festgestellt werden 78. Die körperliche Betätigung, die Erhöhung des Lymphflusses und die Stressreduktion scheinen Yoga zu einer guten Intervention bei Colitis ulcerosa zu machen.
Colitis ulcerosa Gruppe
In unserer Facebookgruppe zu Colitis Ulcerosa können Sie sich mit anderen Colitis-Betroffenen austauschen. Sie finden dort nicht nur weiterführende Informationen über die hier im Beitrag genannten Ursachen, sondern auch Praxistipps für den Alltag.
Colitis ulcerosa – ein Aktionsplan zum Sofort-Starten
Der kleine Aktionsplan kann sofort umgesetzt werden und erleichtert den Start mit einer Schritt-für-Schritt-Anleitung.
- Suchen Sie sich einen Arzt, der die erwähnten Methoden der Schulmedizin und der Naturheilkunde praktiziert und Ihnen so eine optimale Behandlungsgrundlage bietet. Ein funktionell denkender Gastroenterologe eignet sich ebenso wie funktionelle Mediziner und Heilpraktiker. Um einen funktionellen Mediziner in Ihrer Umgebung zu finden, hilft die Google-Suche „Funktionelle Medizin Wohnort“.
- Fahren Sie mit der Ihnen verschriebenen schulmedizinischen Therapie fort und setzen nicht in Eigeninitiative Medikamente ab. Unternehmen Sie Auslassversuche nur in Zusammenarbeit mit einem Arzt oder Heilpraktiker. Bei besserer Symptomatik durch gesunde Ernährung, Lebensführung und Naturheilkunde ist es möglich, die Medikament-Dosierung mit der Zeit zu reduzieren.
- Überprüfen Sie, ob weitere Mitglieder in Ihrem Familienkreis von Colitis ulcerosa oder anderen chronisch-entzündlichen Darmerkrankungen betroffen sind. So können Sie den genetischen Einfluss auf die Krankheitsentstehung einschätzen.
- Überlegen Sie anhand der Colitis ulcerosa Ursachen, was bei Ihnen zu der Erkrankung geführt haben könnte. Versuchen Sie, diese Ursachen mit den genannten Methoden zu beseitigen.
- Ziehen Sie eine Ernährungsumstellung in Erwägung. Dies kann so aussehen, dass Sie schrittweise die empfohlenen Nahrungsmittel aus diesem Beitrag in Ihren Ernährungsalltag einbauen und schadhafte Nahrungsmittel reduzieren. Ein Umstieg auf das Paleo-Autoimmunprotokoll bietet sich ebenfalls an.
- Es ist hilfreich, ein Ernährungstagebuch zu führen, um die Auswirkung bestimmter Nahrungsmittel auf die Gesundheit zu überprüfen.
- Ein großes Blutbild gibt Aufschluss über Entzündungszustände im Inneren und etwaige Nährstoffmängel. Es wird empfohlen mit einem Arzt oder Therapeuten diese Nährstoffmängel zusammen anzugehen und zu beseitigen.
- Mit den genannten Ratschlägen zur Naturheilkunde können Sie abseits von Medikamenten und Ernährung das Krankheitsbild zusätzlich verbessern. Ein funktionell denkender Arzt oder Therapeut hilft Ihnen dabei weiter.
- Vergessen Sie nicht den Faktor der gesunden Lebensführung bei Colitis ulcerosa. Stress, Schlaf, Sport und die Chronobiologie haben ebenfalls Auswirkungen auf die Gesundheit.
Zusammenfassung – Colitis ulcerosa im Überblick
Colitis ulcerosa ist eine Autoimmunerkrankung des Darms, genauer gesagt des Dickdarms. Aus verschiedenen Gründen kommt es zu einer Infektion der Dickdarmschleimhaut mit Bakterien, einer chronischen Entzündung sowie einer Autoimmunreaktion gegen die obere Schleimhaut im Dickdarm.
Die Folgen sind Bauchschmerzen, Bauchkrämpfe, blutiger und schleimiger Durchfall, chronische Müdigkeit und während eines akuten Schubs Fieber und systemische Beschwerden.
Mit Leitlinien und einer mehrschrittigen Diagnose ist eine Colitis ulcerosa Diagnose gut durchführbar und sehr wahrscheinlich. Je nach Lokus und Krankheitsstadium sieht die schulmedizinische Therapie bei Colitis eine Unterdrückung der Entzündung, des Immunsystems sowie Schmerzlinderung vor. Eine langanhaltende Besserung oder gar Remission oder Heilung sieht die Schulmedizin nicht vor.
Die Kombination aus Schulmedizin und Naturheilkunde wird in wissenschaftlichen Studien immer häufiger empfohlen. Denn bestimmte Ernährungsweisen, Nahrungsmittel, Kräuter und Nährstoffpräparate werden mit einer Verbesserung der Symptomatik und in vielen Fällen mit Remission in Verbindung gebracht.
Das Paleo-Autoimmunprotokoll ist eine Ernährungsform, die speziell für Autoimmunerkrankte entwickelt wurde. In einer klinischen Studie gelang es nach 11 Wochen mit dieser Ernährungsform 70 % der Teilnehmer mit Colitis und Morbus Crohn in Remission zu gehen und diese längerfristig aufrechtzuerhalten 19. Das Paleo-Autoimmunprotokoll scheint eine effiziente Ernährungsform bei Colitis zu sein.
Bestimmte Nahrungsmittel stehen mit einer Verbesserung der Krankheit in Verbindung. In der Naturheilkunde gibt es einige Kräuter und Nahrungsergänzungsmittel, die unterstützend wirken, die Lebensqualität der Betroffenen stark verbessern und in vielen Fällen eine Remission (völlige Symptomfreiheit) ermöglichen.
Treten Sie unserer Facebookgruppe zu Colitis ulcerosa bei, um immer auf dem neuesten Stand zu bleiben.
[su_posts template=“templates/list-loop.php“ tax_term=“2514″ order=“desc“ orderby=“rand“]
Wie sind Ihre Erfahrungen mit Colitis ulcerosa? Was hat Ihnen bisher geholfen, was weniger? Wir freuen uns über Ihren Kommentar!
[su_spoiler title=“Quellenverzeichnis“]
Bildquellen: (c) Depositphotos @marina_ua, VadimVasenin, Softlight_69, pathastings, kgtohbu, alexraths
- https://www.dccv.de/
- Loftus, Edward V., JR (2004): Clinical epidemiology of inflammatory bowel disease: Incidence, prevalence, and environmental influences. In: Gastroenterology 126 (6), S. 1504–1517.
- Burisch, Johan; Jess, Tine; Martinato, Matteo; Lakatos, Peter L. (2013): The burden of inflammatory bowel disease in Europe. In: Journal of Crohn’s & colitis 7 (4), S. 322–337. DOI: 10.1016/j.crohns.2013.01.010.
- Xavier, R. J.; Podolsky, D. K. (2007): Unravelling the pathogenesis of inflammatory bowel disease. In: Nature 448 (7152), S. 427–434. DOI: 10.1038/nature06005.
- Pene, Jerome; Chevalier, Sylvie; Preisser, Laurence; Venereau, Emilie; Guilleux, Marie-Helene; Ghannam, Soufiane et al. (2008): Chronically inflamed human tissues are infiltrated by highly differentiated Th17 lymphocytes. In: Journal of immunology (Baltimore, Md. : 1950) 180 (11), S. 7423–7430.
- D’Argenio, Giuseppe; Mazzone, Giovanna; Tuccillo, Concetta; Ribecco, Maria T.; Graziani, Giulia; Gravina, Antonietta G. et al. (2012): Apple polyphenols extract (APE) improves colon damage in a rat model of colitis. In: Digestive and liver disease : official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver 44 (7), S. 555–562. DOI: 10.1016/j.dld.2012.01.009.
- Fyderek, Krzysztof; Strus, Magdalena; Kowalska-Duplaga, Kinga; Gosiewski, Tomasz; Wedrychowicz, Andrzej; Jedynak-Wasowicz, Urszula et al. (2009): Mucosal bacterial microflora and mucus layer thickness in adolescents with inflammatory bowel disease. In: World Journal of Gastroenterology 15 (42), S. 5287–5294.
- Hammer, Heinz F. (2011): Gut microbiota and inflammatory bowel disease. In: Digestive diseases (Basel, Switzerland) 29 (6), S. 550–553. DOI: 10.1159/000332981.
- Badr-el-Din, S.; Trejdosiewicz, L. K.; Heatley, R. V.; Losowsky, M. S. (1988): Local immunity in ulcerative colitis: evidence for defective secretory IgA production. In: Gut 29 (8), S. 1070–1075. gastroenterology 100 (7), S. 1539–1546. DOI: 10.1111/j.1572-0241.2005.41794.x.
- Herfarth, Hans H.; Martin, Christopher F.; Sandler, Robert S.; Kappelman, Michael D.; Long, Millie D. (2014): Prevalence of a gluten-free diet and improvement of clinical symptoms in patients with inflammatory bowel diseases. In: Inflammatory bowel diseases 20 (7), S. 1194–1197. DOI: 10.1097/MIB.0000000000000077.
- Jedel, S.; Hoffman, A.; Merriman, P.; Swanson, B.; Voigt, R.; Rajan, K. B. et al. (2014): A randomized controlled trial of mindfulness-based stress reduction to prevent flare-up in patients with inactive ulcerative colitis. In: Digestion 89 (2), S. 142–155. DOI: 10.1159/000356316.
- Sutherland, L.; Roth, D.; Beck, P.; May, G.; Makiyama, K. (2002): Oral 5-aminosalicylic acid for maintenance of remission in ulcerative colitis. In: The Cochrane database of systematic reviews (4), CD000544. DOI: 10.1002/14651858.CD000544.
- Braly, Kimberly; Williamson, Nila; Shaffer, Michele L.; Lee, Dale; Wahbeh, Ghassan; Klein, Jani et al. (2017): Nutritional Adequacy of the Specific Carbohydrate Diet in Pediatric Inflammatory Bowel Disease. In: Journal of pediatric gastroenterology and nutrition 65 (5), S. 533–538. DOI: 10.1097/MPG.0000000000001613.
- Gearry, Richard B.; Irving, Peter M.; Barrett, Jacqueline S.; Nathan, Debbie M.; Shepherd, Sue J.; Gibson, Peter R. (2009): Reduction of dietary poorly absorbed short-chain carbohydrates (FODMAPs) improves abdominal symptoms in patients with inflammatory bowel disease-a pilot study. In: Journal of Crohn’s & colitis 3 (1), S. 8–14. DOI: 10.1016/j.crohns.2008.09.004.
- Khandalavala, Birgit N.; Nirmalraj, Maya C. (2015): Resolution of Severe Ulcerative Colitis with the Specific Carbohydrate Diet. In: Case reports in gastroenterology 9 (2), S. 291–295. DOI: 10.1159/000438745.
- Dubrovsky A, Kitts CL. Effect of the Specific Carbohydrate Diet on the Microbiome of a Primary Sclerosing Cholangitis and Ulcerative Colitis Patient. Muacevic A, Adler JR, eds. Cureus. 2018;10(2):e2177. doi:10.7759/cureus.2177.
- Durchschein F, Petritsch W, Hammer HF. Diet therapy for inflammatory bowel diseases: The established and the new. World Journal of Gastroenterology. 2016;22(7):2179-2194. doi:10.3748/wjg.v22.i7.2179.
- Koelink, Pim J.; Overbeek, Saskia A.; Braber, Saskia; Morgan, Mary E.; Henricks, Paul A. J.; Abdul Roda, Mojtaba et al. (2014): Collagen degradation and neutrophilic infiltration: a vicious circle in inflammatory bowel disease. In: Gut 63 (4), S. 578–587. DOI: 10.1136/gutjnl-2012-303252.
- Konijeti, Gauree Gupta; Kim, NaMee; Lewis, James D.; Groven, Shauna; Chandrasekaran, Anita; Grandhe, Sirisha et al. (2017): Efficacy of the Autoimmune Protocol Diet for Inflammatory Bowel Disease. In: Inflammatory bowel diseases 23 (11), S. 2054–2060. DOI: 10.1097/MIB.0000000000001221.
- Ham, Maggie; Moss, Alan C. (2012): Mesalamine in the treatment and maintenance of remission of ulcerative colitis. In: Expert review of clinical pharmacology 5 (2), S. 113–123. DOI: 10.1586/ecp.12.2.
- Karner, Max; Kocjan, Andreas; Stein, Juergen; Schreiber, Stefan; Boyen, Georg von; Uebel, Peter et al. (2014): First multicenter study of modified release phosphatidylcholine „LT-02“ in ulcerative colitis: a randomized, placebo-controlled trial in mesalazine-refractory courses. In: The American journal of gastroenterology 109 (7), S. 1041–1051. DOI: 10.1038/ajg.2014.104.
- Lang, Alon; Salomon, Nir; Wu, Justin C. Y.; Kopylov, Uri; Lahat, Adi; Har-Noy, Ofir et al. (2015): Curcumin in Combination With Mesalamine Induces Remission in Patients With Mild-to-Moderate Ulcerative Colitis in a Randomized Controlled Trial. In: Clinical gastroenterology and hepatology : the official clinical practice journal of the American Gastroenterological Association 13 (8), 1444-9.e1. DOI: 10.1016/j.cgh.2015.02.019.
- Lewis, James D.; Lichtenstein, Gary R.; Deren, Julius J.; Sands, Bruce E.; Hanauer, Stephen B.; Katz, Jeffrey A. et al. (2008): Rosiglitazone for active ulcerative colitis: a randomized placebo-controlled trial. In: Gastroenterology 134 (3), S. 688–695. DOI: 10.1053/j.gastro.2007.12.012.
- Lewis, J. D.; Lichtenstein, G. R.; Stein, R. B.; Deren, J. J.; Judge, T. A.; Fogt, F. et al. (2001): An open-label trial of the PPAR-gamma ligand rosiglitazone for active ulcerative colitis. In: The American journal of gastroenterology 96 (12), S. 3323–3328. DOI: 10.1111/j.1572-0241.2001.05333.x.
- Shibolet, O.; Regushevskaya, E.; Brezis, M.; Soares-Weiser, K. (2005): Cyclosporine A for induction of remission in severe ulcerative colitis. In: The Cochrane database of systematic reviews (1), CD004277. DOI: 10.1002/14651858.CD004277.pub2.
- Liu, W.; Wang, J.; Wang, H.; Chen, X. Y.; Li, J. S. (2018): The impact of stress and personality on resilience of patients with ulcerative colitis. In: Zhonghua nei ke za zhi 57 (2), S. 107–111. DOI: 10.3760/cma.j.issn.0578-1426.2018.02.005.
- Mehta, Minesh; Ahmed, Shifat; Dryden, Gerald (2018): Refractory pouchitis improves after administration of the green tea polyphenol EGCG: a retrospective review. In: International journal of colorectal disease 33 (1), S. 83–86. DOI: 10.1007/s00384-017-2906-5.
- Bing, Xue; Xuelei, Liu; Wanwei, Dong; Linlang, Liang; Keyan, Chen (2017): EGCG Maintains Th1/Th2 Balance and Mitigates Ulcerative Colitis Induced by Dextran Sulfate Sodium through TLR4/MyD88/NF-kappaB Signaling Pathway in Rats. In: Canadian journal of gastroenterology & hepatology 2017, S. 3057268. DOI: 10.1155/2017/3057268.
- Ananthakrishnan, Ashwin N.; Higuchi, Leslie M.; Huang, Edward S.; Khalili, Hamed; Richter, James M.; Fuchs, Charles S.; Chan, Andrew T. (2012): Aspirin, nonsteroidal anti-inflammatory drug use, and risk for Crohn disease and ulcerative colitis: a cohort study. In: Annals of internal medicine 156 (5), S. 350–359. DOI: 10.7326/0003-4819-156-5-201203060-00007.
- Mijan, Mohammad Al; Lim, Beong Ou (2018): Diets, functional foods, and nutraceuticals as alternative therapies for inflammatory bowel disease: Present status and future trends. In: World Journal of Gastroenterology 24 (25), S. 2673–2685. DOI: 10.3748/wjg.v24.i25.2673.
- Hou, Jason K.; Lee, Dale; Lewis, James (2014): Diet and Inflammatory Bowel Disease: Review of Patient-Targeted Recommendations. In: Clinical Gastroenterology and Hepatology 12 (10), S. 1592–1600. DOI: 10.1016/j.cgh.2013.09.063.
- Nie, Jia-Yan; Zhao, Qiu (2017): Beverage consumption and risk of ulcerative colitis: Systematic review and meta-analysis of epidemiological studies. In: Medicine 96 (49), e9070. DOI: 10.1097/MD.0000000000009070.
- Pervin, Mehnaz; Hasnat, Md Abul; Lim, Ji-Hong; Lee, Yoon-Mi; Kim, Eun Ok; Um, Byung-Hun; Lim, Beong Ou (2016): Preventive and therapeutic effects of blueberry (Vaccinium corymbosum) extract against DSS-induced ulcerative colitis by regulation of antioxidant and inflammatory mediators. In: The Journal of nutritional biochemistry 28, S. 103–113. DOI: 10.1016/j.jnutbio.2015.10.006.
- Ramadass, Satiesh Kumar; Jabaris, Sugin Lal; Perumal, Ramesh Kannan; HairulIslam, Villianur Ibrahim; Gopinath, Arun; Madhan, Balaraman (2016): Type I collagen and its daughter peptides for targeting mucosal healing in ulcerative colitis: A new treatment strategy. In: European journal of pharmaceutical sciences : official journal of the European Federation for Pharmaceutical Sciences 91, S. 216–224. DOI: 10.1016/j.ejps.2016.05.015.
- Rogler, Gerhard; Zeitz, Jonas; Biedermann, Luc (2016): The Search for Causative Environmental Factors in Inflammatory Bowel Disease. In: Digestive diseases (Basel, Switzerland) 34 Suppl 1, S. 48–55. DOI: 10.1159/000447283.
- Rosillo, Maria Angeles; Sanchez-Hidalgo, Marina; Cardeno, Ana; Aparicio-Soto, Marina; Sanchez-Fidalgo, Susana; Villegas, Isabel; de la Lastra, Catalina Alarcon (2012): Dietary supplementation of an ellagic acid-enriched pomegranate extract attenuates chronic colonic inflammation in rats. In: Pharmacological research 66 (3), S. 235–242. DOI: 10.1016/j.phrs.2012.05.006.
- Bassaganya-Riera, Josep; DiGuardo, Margaret; Climent, Montse; Vives, Cristina; Carbo, Adria; Jouni, Zeina E. et al. (2011): Activation of PPARgamma and delta by dietary punicic acid ameliorates intestinal inflammation in mice. In: The British journal of nutrition 106 (6), S. 878–886. DOI: 10.1017/S0007114511001188.
- Bassaganya-Riera, Josep; Viladomiu, Monica; Pedragosa, Mireia; Simone, Claudio de; Hontecillas, Raquel (2012): Immunoregulatory mechanisms underlying prevention of colitis-associated colorectal cancer by probiotic bacteria. In: PloS one 7 (4), e34676. DOI: 10.1371/journal.pone.0034676.
- Bibiloni, Rodrigo; Fedorak, Richard N.; Tannock, Gerald W.; Madsen, Karen L.; Gionchetti, Paolo; Campieri, Massimo et al. (2005): VSL#3 probiotic-mixture induces remission in patients with active ulcerative colitis. In: The American journal of
- Collado, M. C.; Meriluoto, J.; Salminen, S. (2007): Role of commercial probiotic strains against human pathogen adhesion to intestinal mucus. In: Letters in applied microbiology 45 (4), S. 454–460. DOI: 10.1111/j.1472-765X.2007.02212.x.
- Madsen, K.; Cornish, A.; Soper, P.; McKaigney, C.; Jijon, H.; Yachimec, C. et al. (2001): Probiotic bacteria enhance murine and human intestinal epithelial barrier function. In: Gastroenterology 121 (3), S. 580–591.
- Shang, Mei; Sun, Jun (2017): Vitamin D/VDR, probiotics, and gastrointestinal diseases. In: Current medicinal chemistry 24 (9), S. 876–887. DOI: 10.2174/0929867323666161202150008.
- Bassaganya-Riera, Josep; Viladomiu, Monica; Pedragosa, Mireia; Simone, Claudio de; Carbo, Adria; Shaykhutdinov, Rustem et al. (2012): Probiotic bacteria produce conjugated linoleic acid locally in the gut that targets macrophage PPAR gamma to suppress colitis. In: PloS one 7 (2), e31238. DOI: 10.1371/journal.pone.0031238.
- Goncalves; Menezes, Zelia; Pereira, Solange Silveira; Alves, Andrea Catao et al. (2013): Gluten-free diet reduces adiposity, inflammation and insulin resistance associated with the induction of PPAR-alpha and PPAR-gamma expression. In: The Journal of nutritional biochemistry 24 (6), S. 1105–1111. DOI: 10.1016/j.jnutbio.2012.08.009.
- Soares, Fabiola Lacerda Pires; Oliveira Matoso, Rafael de; Teixeira, Lilian
- Kudva, Avinash K.; Shay, Ashley E.; Prabhu, K. Sandeep (2015): Selenium and inflammatory bowel disease. In: American journal of physiology. Gastrointestinal and liver physiology 309 (2), G71-7. DOI: 10.1152/ajpgi.00379.2014.
- Speckmann, Bodo; Steinbrenner, Holger (2014): Selenium and selenoproteins in inflammatory bowel diseases and experimental colitis. In: Inflammatory bowel diseases 20 (6), S. 1110–1119. DOI: 10.1097/MIB.0000000000000020.
- Hsiang, Chien-Yun; Lo, Hsin-Yi; Huang, Hui-Chi; Li, Chia-Cheng; Wu, Shih-Lu; Ho, Tin-Yun (2013): Ginger extract and zingerone ameliorated trinitrobenzene sulphonic acid-induced colitis in mice via modulation of nuclear factor-kappaB activity and interleukin-1beta signalling pathway. In: Food chemistry 136 (1), S. 170–177. DOI: 10.1016/j.foodchem.2012.07.124.
- Triantafyllidi, Aikaterini; Xanthos, Theodoros; Papalois, Apostolos; Triantafillidis, John K. (2015 Apr-Jun): Herbal and plant therapy in patients with inflammatory bowel disease. Greece.
- Ley, M. de; Vos, R. de; Hommes, D. W.; Stokkers, P. (2007): Fish oil for induction of remission in ulcerative colitis. In: The Cochrane database of systematic reviews (4), CD005986. DOI: 10.1002/14651858.CD005986.pub2.
- Scaioli, Eleonora; Liverani, Elisa; Belluzzi, Andrea (2017): The Imbalance between n-6/n-3 Polyunsaturated Fatty Acids and Inflammatory Bowel Disease: A Comprehensive Review and Future Therapeutic Perspectives. In: International Journal of Molecular Sciences 18 (12). DOI: 10.3390/ijms18122619.
- Bassaganya-Riera, Josep; Hontecillas, Raquel (2010): Dietary conjugated linoleic acid and n-3 polyunsaturated fatty acids in inflammatory bowel disease. In: Current opinion in clinical nutrition and metabolic care 13 (5), S. 569–573. DOI: 10.1097/MCO.0b013e32833b648e.
- Bassaganya-Riera, Josep; Hontecillas, Raquel (2006): CLA and n-3 PUFA differentially modulate clinical activity and colonic PPAR-responsive gene expression in a pig model of experimental IBD. In: Clinical nutrition (Edinburgh, Scotland) 25 (3), S. 454–465. DOI: 10.1016/j.clnu.2005.12.008.
- Uchiyama, Kan; Nakamura, Makoto; Odahara, Shunichi; Koido, Shigeo; Katahira, Kiyohiko; Shiraishi, Hiromi et al. (2010): N-3 polyunsaturated fatty acid diet therapy for patients with inflammatory bowel disease. In: Inflammatory bowel diseases 16 (10), S. 1696–1707. DOI: 10.1002/ibd.21251.
- Valcheva-Kuzmanova, Stefka; Kuzmanov, Atanas; Kuzmanova, Vasilena; Tzaneva, Maria (2018): Aronia melanocarpa fruit juice ameliorates the symptoms of inflammatory bowel disease in TNBS-induced colitis in rats. In: Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 113, S. 33–39. DOI: 10.1016/j.fct.2018.01.011.
- Wagner, Anika E.; Will, Olga; Sturm, Christine; Lipinski, Simone; Rosenstiel, Philip; Rimbach, Gerald (2013): DSS-induced acute colitis in C57BL/6 mice is mitigated by sulforaphane pre-treatment. In: The Journal of nutritional biochemistry 24 (12), S. 2085–2091. DOI: 10.1016/j.jnutbio.2013.07.009.
- Wang, Qingjing; Hou, Yongqing; Yi, Dan; Wang, Lei; Ding, Binying; Chen, Xing et al. (2013): Protective effects of N-acetylcysteine on acetic acid-induced colitis in a porcine model. In: BMC gastroenterology 13, S. 133. DOI: 10.1186/1471-230X-13-133.
- Hou, Yongqing; Wang, Lei; Yi, Dan; Wu, Guoyao (2015): N-acetylcysteine and intestinal health: a focus on its mechanism of action. In: Frontiers in bioscience (Landmark edition) 20, S. 872–891.
- Gupta, I.; Parihar, A.; Malhotra, P.; Gupta, S.; Ludtke, R.; Safayhi, H.; Ammon, H. P. (2001): Effects of gum resin of Boswellia serrata in patients with chronic colitis. In: Planta medica 67 (5), S. 391–395. DOI: 10.1055/s-2001-15802.
- Weisshof, Roni; Chermesh, Irit (2015): Micronutrient deficiencies in inflammatory bowel disease. In: Current opinion in clinical nutrition and metabolic care 18 (6), S. 576–581. DOI: 10.1097/MCO.0000000000000226.
- Xiao, Xiao; Kim, Jonggun; Sun, Quancai; Kim, Daeyoung; Park, Cheon-Seok; Lu, Tzong-Shi; Park, Yeonhwa (2015): Preventive effects of cranberry products on experimental colitis induced by dextran sulphate sodium in mice. In: Food chemistry 167, S. 438–446. DOI: 10.1016/j.foodchem.2014.07.006.
- Zezos, Petros; Saibil, Fred (2015 Aug 7): Inflammatory pouch disease: The spectrum of pouchitis. United States.
- Zhang, Dingguo; Wei, Cheng; Yao, Jun; Cai, Xiaoyan; Wang, Lisheng (2015): Interleukin-10 gene-carrying bifidobacteria ameliorate murine ulcerative colitis by regulating regulatory T cell/T helper 17 cell pathway. In: Experimental biology and medicine (Maywood, N.J.) 240 (12), S. 1622–1629. DOI: 10.1177/1535370215584901.
- Zhu, Guo; Wang, Huanan; Wang, Tiancheng; Shi, Fushan (2017): Ginsenoside Rg1 attenuates the inflammatory response in DSS-induced mice colitis. In: International immunopharmacology 50, S. 1–5. DOI: 10.1016/j.intimp.2017.06.002.
- Zittan, Eran; Kelly, Orlaith B.; Kirsch, Richard; Milgrom, Raquel; Burns, Jane; Nguyen, Geoffrey C. et al. (2016): Low Fecal Calprotectin Correlates with Histological Remission and Mucosal Healing in Ulcerative Colitis and Colonic Crohn’s Disease. In: Inflammatory bowel diseases 22 (3), S. 623–630. DOI: 10.1097/MIB.0000000000000652.
- Vestergaard, P. (2004): Prevalence and pathogenesis of osteoporosis in patients with inflammatory bowel disease. In: Minerva medica 95 (6), S. 469–480.
- Kuwabara, A.; Tanaka, K.; Tsugawa, N.; Nakase, H.; Tsuji, H.; Shide, K. et al. (2009): High prevalence of vitamin K and D deficiency and decreased BMD in inflammatory bowel disease. In: Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA 20 (6), S. 935–942. DOI: 10.1007/s00198-008-0764-2.
- Nakajima, Sachiko; Iijima, Hideki; Egawa, Satoshi; Shinzaki, Shinichiro; Kondo, Jumpei; Inoue, Takahiro et al. (2011): Association of vitamin K deficiency with bone metabolism and clinical disease activity in inflammatory bowel disease. In: Nutrition (Burbank, Los Angeles County, Calif.) 27 (10), S. 1023–1028. DOI: 10.1016/j.nut.2010.10.021.
- Nowak, Jan K.; Grzybowska-Chlebowczyk, Urszula; Landowski, Piotr; Szaflarska-Poplawska, Anna; Klincewicz, Beata; Adamczak, Daria et al. (2014): Prevalence and correlates of vitamin K deficiency in children with inflammatory bowel disease. In: Scientific reports 4, S. 4768. DOI: 10.1038/srep04768.
- Fabisiak, Natalia; Fabisiak, Adam; Watala, Cezary; Fichna, Jakub (2017): Fat-soluble Vitamin Deficiencies and Inflammatory Bowel Disease: Systematic Review and Meta-Analysis. In: Journal of clinical gastroenterology 51 (10), S. 878–889. DOI: 10.1097/MCG.0000000000000911.
- Gubatan, John; Mitsuhashi, Shuji; Zenlea, Talia; Rosenberg, Laura; Robson, Simon; Moss, Alan C. (2017): Low Serum Vitamin D During Remission Increases Risk of Clinical Relapse in Patients With Ulcerative Colitis. In: Clinical gastroenterology and hepatology : the official clinical practice journal of the American Gastroenterological Association 15 (2), 240-246.e1. DOI: 10.1016/j.cgh.2016.05.035.
- Meckel, Katherine; Li, Yan Chun; Lim, John; Kocherginsky, Masha; Weber, Chris; Almoghrabi, Anas et al. (2016): Serum 25-hydroxyvitamin D concentration is inversely associated with mucosal inflammation in patients with ulcerative colitis. In: The American journal of clinical nutrition 104 (1), S. 113–120. DOI: 10.3945/ajcn.115.123786.
- Dundar, Emine; Olgun, Esra Gurlek; Isiksoy, Serap; Kurkcuoglu, Mine; Baser, K. Husnu Can; Bal, Cengiz (2008): The effects of intra-rectal and intra-peritoneal application of Origanum onites L. essential oil on 2,4,6-trinitrobenzenesulfonic acid-induced colitis in the rat. In: Experimental and toxicologic pathology : official journal of the Gesellschaft fur Toxikologische Pathologie 59 (6), S. 399–408. DOI: 10.1016/j.etp.2007.11.009.
- Minaiyan, M.; Ghannadi, A. R.; Afsharipour, M.; Mahzouni, P. (2011): Effects of extract and essential oil of Rosmarinus officinalis L. on TNBS-induced colitis in rats. In: Research in pharmaceutical sciences 6 (1), S. 13–21.
- Rashidian, Amir; Roohi, Parnia; Mehrzadi, Saeed; Ghannadi, Ali Reza; Minaiyan, Mohsen (2016): Protective Effect of Ocimum basilicum Essential Oil Against Acetic Acid-Induced Colitis in Rats. In: Journal of evidence-based complementary & alternative medicine 21 (4), NP36-42. DOI: 10.1177/2156587215616550.
- Rezayat, Seyed Mahdi; Dehpour, Ahmad-Reza; Motamed, Saeed Mohammadi; Yazdanparast, Maryam; Chamanara, Mohsen; Sahebgharani, Mousa; Rashidian, Amir (2018): Foeniculum vulgare essential oil ameliorates acetic acid-induced colitis in rats through the inhibition of NF-kB pathway. In: Inflammopharmacology 26 (3), S. 851–859. DOI: 10.1007/s10787-017-0409-1.
- Yu, Xiuting; Yang, Guanghua; Jiang, Hua; Lin, Shuhai; Liu, Yuhong; Zhang, Xie et al. (2017): Patchouli oil ameliorates acute colitis: A targeted metabolite analysis of 2,4,6-trinitrobenzenesulfonic acid-induced rats. In: Experimental and therapeutic medicine 14 (2), S. 1184–1192. DOI: 10.3892/etm.2017.4577.
- Purnima Sharma, Gopal Poojary, Sada Nand Dwivedi, and Kishore Kumar Deepak (2015) Effect of Yoga-Based Intervention in Patients with Inflammatory Bowel Disease. International Journal of Yoga Therapy: 2015, Vol. 25, No. 1, pp. 101-112.
- Weiss, Scott T. (2002): Eat dirt–the hygiene hypothesis and allergic diseases. In: The New England journal of medicine 347 (12), S. 930–931. DOI: 10.1056/NEJMe020092.
- Halme L, Paavola-Sakki P, Turunen U, Lappalainen M, Färkkilä M, Kontula K. Family and twin studies in inflammatory bowel disease. World Journal of Gastroenterology : WJG. 2006;12(23):3668-3672. doi:10.3748/wjg.v12.i23.3668.
- Dietary Salt Exacerbates Experimental Colitis Alan L. Tubbs, Bo Liu, Troy D. Rogers, R. Balfour Sartor and Edward A. Miao J Immunol August 1, 2017, 199 (3) 1051-1059; DOI: https://doi.org/10.4049/jimmunol.1700356
-
Ananthakrishnan AN, Khalili H, Konijeti GG, et alLong-term intake of dietary fat and risk of ulcerative colitis and Crohn’s diseaseGut 2014;63:776-784.
- Molodecky et al. (2012): Increasing Incidence and Prevalence of the Inflammatory Bowel Diseases With Time, Based on Systematic Review
- Lewis & Abreu, Diet as a Trigger or Therapy for Inflammatory Bowel Diseases, Gastroenterology Volume 152, Issue 2, January 2017, Pages 398-414.e6
[/su_spoiler]